Uno degli argomenti che ha attirato maggiormente la mia attenzione negli ultimi anni è il legame fra stato nutrizionale e patologie della donna. E poiché la menopausa è una fase della vita in cui la donna va incontro a moltissimi cambiamenti che possono renderne la salute più fragile, le mie letture si sono orientate in quel senso. Questo è il primo di una serie di articoli che tratteranno dell’influenza degli stili di vita sulla salute della donna in menopausa, con i quali proverò a guidarvi nell’acquisizione di abitudini alimentari (e non) più sane e preventive.
Uno degli argomenti che ha attirato maggiormente la mia attenzione negli ultimi anni è il legame fra stato nutrizionale e patologie della donna. E poiché la menopausa è una fase della vita in cui la donna va incontro a moltissimi cambiamenti che possono renderne la salute più fragile, le mie letture si sono orientate in quel senso. Questo è il primo di una serie di articoli che tratteranno dell’influenza degli stili di vita sulla salute della donna in menopausa, con i quali proverò a guidarvi nell’acquisizione di abitudini alimentari (e non) più sane e preventive.
********************************************************************************
Introduzione
Molti studi evidenziano che in menopausa sono richieste attenzioni particolari all’aspetto nutrizionale: questa condizione ormonale modifica infatti molti aspetti della salute femminile, ponendo la donna in una condizione di maggiore fragilità rispetto ad alcune patologie.
Il periodo che precede la menopausa perciò diventa un’importante occasione per migliorare le proprie abitudini alimentari e di attività fisica, in modo da ottimizzare lo stato di salute per gli anni a venire.
In generale, i principali problemi cui una donna va incontro nel periodo della menopausa e in quello successivo sono legati all’aumento di peso, alla perdita di massa ossea e muscolare, all’osteoporosi e un aumento del rischio di malattie cardiovascolari. Inoltre, con l’allungamento della vita media, è aumentato anche l’impatto di alcune patologie metaboliche e neurodegenerative, in particolare il disturbo depressivo maggiore e il morbo di Alzheimer, già di per sé più diffusi nelle donne e maggiormente presenti in menopausa (Dai un’occhiata a questi dati). Il meccanismo che sta emergendo sempre più chiaramente dalle ricerche su questa fase ormonale e il suo corredo di rischio patologico – sia metabolico che scheletrico, cardiologico e neurologico – è rappresentato dall’infiammazione sistemica di basso grado, che però è suscettibile (buona notizia!) ai cambiamenti dello stile di vita, comprese le abitudini alimentari.
Oltre alla maggiore longevità rispetto agli uomini, la vulnerabilità delle donne in menopausa è stata collegata a ulteriori fattori, come influenze genetiche, modificazioni ormonali, determinanti socio-culturali (istruzione e stato occupazionale, storia riproduttiva) [1, 2].
Come già accennato, l’alimentazione rappresenta un fattore critico, sia come rischio modificabile che come mediatore dell’infiammazione e dell’intensità di alcuni sintomi. La dieta occidentale, uno dei modelli alimentari più diffusi a livello mondiale e caratterizzato da un elevato apporto di grassi saturi e trans, un elevato rapporto omega-6/3, carboidrati raffinati, zuccheri, sale e alimenti ultra-processati, è fortemente associata a elevati livelli di marcatori infiammatori come la proteina C-reattiva (PCR) [3, 4]. Allo stesso tempo, essa è carente di fattori ad azione antinfiammatoria, tra cui fibre alimentari, acidi grassi omega-3 e -9, antiossidanti. È noto che stress, umore disfunzionale e scarsa qualità del sonno, molto frequenti in menopausa, possono determinare preferenze per cibi molto palatabili, ricchi di zuccheri e grassi, esacerbando così il potenziale infiammatorio della dieta occidentale.
Alimentazione e disturbi dell’umore e del sonno
Il desiderio di snack e dolci quando ci si sente ansiosi o depressi è una caratteristica comune alle donne in menopausa [5, 6]. In questa fase ormonale, i disturbi del sonno e dell’umore rendono le donne maggiormente suscettibili al consumo di alimenti ad alta densità energetica immediata [7], in particolare quelli ad alto indice glicemico.
I cibi ad alto indice glicemico hanno la capacità di aumentare rapidamente la glicemia e innescare un picco di insulinemia, favorendo l’accumulo di glucosio nelle cellule e portando ad un aumento di peso, (vedi Focus sugli zuccheri e sul confort food). L’alta palatabilità del confort food è stata associata al rilascio di endorfine, con conseguente amplificazione del circuito di ricompensa e sensazione di piacere [8]. Ulteriori studi hanno dimostrato che anche il glucosio ha la capacità di innescare il rilascio di dopamina insieme alle endorfine nel cervello [9]. Dato che la menopausa di per sé è associata a una diminuzione del livello di oppioidi, questa condizione potrebbe contribuire a favorire la plus-richiesta di glucosio. L’assunzione intermittente e frequente di glucosio può portare a una dipendenza da zucchero [10, 11].
Riduzione dei livelli di estrogeni: conseguenze sul metabolismo e sul peso
La riduzione di estrogeni che si verifica in menopausa ha un impatto diretto sul metabolismo lipidico, il consumo di energia e l’accumulo di massa grassa nei distretti addominali/viscerali. È stato ampiamente dimostrato come questa fase sia associata all’aumento di peso.
Cosa ci dicono in tal senso gli studi più importanti? Lo studio SWAN ci dice che le donne di mezza età subiscono una redistrubuzione del grasso corporeo, che l’accumulo è maggiore nella post menopausa piuttosto che nella pre menopausa e che le donne studiate hanno guadagnato in media 0,7 kg all’anno. Il Nurse Health Study registra invece una media di 3 kg in più in 8 anni di follow-up, per una media di 0,4 kg l’anno. Nel complesso, la massa magra (muscoli e ossa) diminuisce, mentre la massa grassa aumenta, in particolare quella addominale, che agendo come organo endocrino innesca il rilascio di citochine proinfiammatorie, oltre a favorire comorbidità cardiache e metaboliche [12]. E’ importante sottolineare, però, che la menopausa non è il solo fattore di rischio di obesità nelle donne, ma che quest’ultima risulta essere associata a sintomi della menopausa più intensi (valutati dall’indice della menopausa di Blatt-Kupperman o dal questionario sulla qualità della vita specifico per la menopausa, MENQOL *).
Tuttavia, gli studi relativi all’influenza della modificazione dietetica sull’aumento di peso in menopausa ci lasciano qualche dubbio riguardo alla sua esclusiva responsabilità. Sembra invece che l’ipotesi più corretta possa essere associata a un rallentamento metabolico e a un potenziale aumento degli spuntini altamente calorici durante la transizione dall’età fertile alla menopausa, fattori che potrebbero produrre un graduale aumento di peso. Questa ipotesi sarebbe coerente col fatto che piccoli e specifici cambiamenti nel comportamento alimentare potrebbero rimanere scarsamente rilevati dai comuni strumenti di indagine e restare così sottostimati [13, 14].
Alimentazione e infiammazione.
Una dieta ricca di zuccheri è stata ampiamente associata all’infiammazione sistemica che porta a disfunzioni del sistema immunitario e/o all’alterazione della permeabilità intestinale [15]. Quando parliamo di zuccheri alimentari, ci riferiamo soprattutto al saccarosio, disaccaride composto da una molecola di glucosio e una di fruttosio. Questi due monosaccaridi sono isomeri (cioè, hanno la stessa formula molecolare, con differente disposizione degli atomi nello spazio), ma presentano un metabolismo differente. In particolare, il fruttosio ingerito, al contrario del glucosio, non provoca secrezione diretta di insulina e non ha bisogno di questo ormone per entrare nelle cellule; pertanto, il suo metabolismo non è regolato da alcun feed-back.
Inoltre, gli zuccheri alimentari, e il fruttosio in particolare, hanno la capacità di promuovere la sintesi de novo di acidi grassi liberi [16] e la conseguente produzione di grassi di accumulo, oltre che di sottoprodotti metabolici come il lattato o l’acido urico, capaci a loro volta produrre stress ossidativo e infiammazione [17]. Un altro fenomeno legato all’eccesso di fruttosio è la glicosilazione avanzata, con liberazione di prodotti metabolici tossici, prevalentemente proteine glicosilate, il cui accumulo è associato allo stress ossidativo e all’infiammazione [18]. Inoltre, una dieta ricca di fruttosio e saccarosio induce stress ossidativo nel reticolo endoplasmatico delle cellule intestinali, portando a un “allentamento” delle giunzioni strette fra gli enterociti e quindi a un aumento della permeabilità intestinale, con conseguente disregolazione immunologica [19].
Anche il glucosio, sebbene sia essenziale per una corretta funzione immunitaria, ad alte dosi ha un effetto deleterio sulle stesse cellule immunitarie [20], in quanto fattore scatenante del citochine pro-infiammatorie. Nonostante i diversi percorsi metabolici, fruttosio e glucosio sembrano quindi essere ugualmente coinvolti nei fenomeni proinfiammatori.
È interessante notare che gli zuccheri aggiunti provenienti dalle bevande edulcorate, indipendentemente dalla loro natura, sono stati associati a una maggiore presenza di marcatori infiammatori e a un maggiore picco glicemico rispetto a quello generato dagli zuccheri presenti negli alimenti [21]. E’ noto da tempo che gli zuccheri raffinati e con indice glicemico elevato (tipicamente presenti nelle comuni bevande edulcorate) sono associati allo stress ossidativo, all’attivazione di vari percorsi pro-infiammatori e ai marcatori infiammatori elevati (come la proteina C reattiva). Al contrario, i carboidrati a basso indice glicemico (complessi e da fonti integrali) sono associati a una diminuzione del livello di indici infiammatori [22].
Anche i grassi alimentari hanno effetti pro-infiammatori. È stato dimostrato che gli acidi grassi saturi (SFA) sono associati all’infiammazione attraverso diverse vie: in particolare, l’attivazione di recettori di membrana coinvolti nella risposta immunitaria innata, la produzione di ceramide (particolari molecole lipidiche della membrana cellulare) e la formazione di grosse strutture lipidiche. Una dieta ricca di grassi è peraltro associata a un elevato passaggio di lipopolisaccaride batterico (LPS) attraverso la parete intestinale. Il LPS può attraversare la barriera intestinale attraverso vie transcellulari (chilomicroni, assorbimento lipidico) o vie paracellulari come avviene nell’intestino permeabile [23]. Una dieta ricca di grassi può portare, fra gli altri effetti, all’accumulo intracellulare di acido palmitico che genera la produzione di specie reattive dell’ossigeno (ROS) e il rilascio di proteine pro-infiammatorie. Allo stesso modo, gli acidi grassi trans, che provengono principalmente da grassi idrogenati dei cibi industriali e dalla cottura prolungata degli oli vegetali, sono associati all’attivazione di vie pro-infiammatorie e all’aumento di marcatori come la proteina C reattiva [24]. Infine, due parole su omega 6 e omega 3: gli acidi grassi polinsaturi n-6, i cosiddetti omega-6, sono precursori delle prostaglandine e leucotrieni, molecole essenziali per l’insorgenza dell’infiammazione. Al contrario, gli omega-3, hanno proprietà antinfiammatorie e sono i precursori di mediatori dello “spegnimento” del processo infiammatorio. Un elevato rapporto n-6/n-3, tipico delle diete occidentali, contribuisce al mantenimento e all’amplificazione del quadro infiammatorio [25 , 26, 27].
Dieta e permeabilità intestinale
Fondamentale per il nostro sistema immunitario risulta essere l’integrità della parete intestinale, che si basa, in particolare, sui seguenti fattori: lo spessore del muco intestinale (barriera fisica che protegge gli enterociti) e l’integrità delle giunzioni strette. Quando questa barriera è danneggiata (intestino permeabile) si verifica il passaggio di endotossine o PAMP (Pathogen Associated Molecular Patterns, come l’LPS) nel tessuto sottoepiteliale e nel flusso sanguigno sottostante, il che porta a infiammazione locale e sistemica [28, 29].
Il microbiota intestinale è definito dai microrganismi (principalmente batteri) che sono ospitati e vivono in simbiosi nel nostro tratto intestinale. La biodiversità e l’abbondanza del microbiota sono protettive per la nostra salute: alcune specie batteriche possono aumentare (tra gli altri benefici) lo spessore del muco intestinale, promuovere la funzionalità e l’aumento delle giunzioni strette, oltre al rilascio di acidi grassi corti (SCFA) – acetato, propionato e butirrato. Questi prodotti metabolici hanno un ruolo trofico per gli enterociti (soprattutto il butirrato), in quanto migliorano la funzione di barriera intestinale, favoriscono l’espressione delle giunzioni strette ed esprimono proprietà antinfiammatorie [30, 31, 32].
La disbiosi intestinale, definita come disequilibrio batterico sia qualitativo che quantitativo, si verifica con maggiore frequenza negli individui anziani; questa evenienza è coerente con il fatto che l’invecchiamento è legato all’infiammazione cronica, o “inflammaging”, considerata un fattore di rischio per varie malattie [33]. La composizione del microbiota è fortemente influenzata anche dall’assunzione alimentare: una dieta ricca di fruttosio porta a disbiosi con una riduzione dei batteri produttori di butirrato e aumento di batteri Gram-negativi, portatori di LPS [34, 35].
Ma di cosa si nutrono i nostri batteri?
La fibra alimentare derivata da alimenti di origine vegetale è il principale substrato del microbiota intestinale, modulando la diversità e l’abbondanza delle specie batteriche: il ruolo protettivo di una dieta ricca di fibre per la salute generale e l’integrità intestinale è ben documentato [36]. Al contrario, il basso apporto di fibre, caratteristico della dieta occidentale, è stato associato alla disbiosi, all’alterazione della permeabilità intestinale e alla successiva infiammazione di basso grado [37].
Dieta e neurogenerazione
L’alimentazione occidentale con il suo apporto infiammatorio è associata a disturbi dell’umore, del sonno e dell’ansia, condizioni che danneggiano la permeabilità intestinale e a lungo andare diventano fattori di rischio per lo sviluppo di patologie psichiatriche e neurodegenerative [38]
Nei modelli animali, gli studi hanno dimostrato che gli stress (psicologici, fisici o sociali) portano a un aumento della permeabilità intestinale. Attraverso la produzione di cortisolo, lo stress provoca un aumento della disponibilità di nutrienti, acqua ed elettroliti (incluso il sodio) che possono aiutare l’organismo a far fronte al presunto “pericolo”. A causa della connessione umorale (ad esempio attraverso catecolamine, cortisolo) e nervosa (fibre nervose simpatiche adrenergiche) tra l’intestino e il cervello, l’aumentata disponibilità di acidi grassi può contribuire ad aumentare la permeabilità intestinale, consentendo il trasferimento di endotossine con l’innesco successivo di un’infiammazione di basso grado [39].
Di recente è stato stabilita una forte connessione tra disturbi del sonno e infiammazione sistemica di basso grado, mediata da una serie di percorsi organici e sistemici interconnessi. Questi includono disregolazione immunitaria, squilibri ormonali e alterazioni metaboliche. I disturbi cronici del sonno sono infatti collegati a livelli elevati di marcatori infiammatori come PCR, interleuchina-6 (IL-6), fattore di necrosi tumorale alfa (TNF-α) e all’aumento di cortisolo [40].
Conclusioni
La menopausa è un periodo critico nella vita di una donna che si estende ben oltre l’invecchiamento riproduttivo, comprendendo profondi cambiamenti ormonali, metabolici e neurobiologici. Nuove evidenze sottolineano il ruolo dell’infiammazione cronica di basso grado come filo conduttore che la menopausa a una maggiore suscettibilità a varie patologie, compresi depressione maggiore e a malattie neurodegenerative. I comportamenti alimentari, in particolare l’adozione di un modello alimentare occidentale, possono esacerbare questo stato infiammatorio, contribuendo alla disregolazione metabolica e alterando l’asse intestino-cervello. Questi fattori combinati possono, nel tempo, compromettere la funzione cognitiva e la salute mentale.
Ad oggi lo stile di vita rappresenta ancora e sempre di più il fattore preventivo più potente, oltre che più economico.
Nei prossimi articoli vedremo nel dettaglio il ruolo dell’alimentazione prevalentemente vegetale e a basso impatto infiammatorio.
*Entrambi i questionari contengono criteri di disturbo dell’umore e del sonno e di compromissione cognitiva.
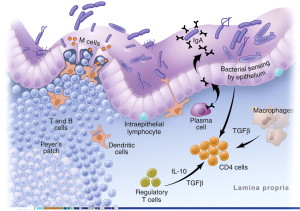



 alcuni fattori associati allo sviluppo di IBD possano essere rappresentati da sollecitazioni eccessive o effetti negativi sul microbiota. I fattori ambientali che possono alterarne la composizione comprendono la dieta, l’uso di antibiotici e l’area geografica. La nota “ipotesi dell’igiene” suggerisce che gli esseri umani che vivono nei paesi più industrializzati sono esposti sin dalla primissima infanzia a un minor numero di microbi che porta allo sviluppo di un sistema immunitario meno in grado di “tollerare” l’esposizione all’ambiente microbico in età avanzata. Questo può attivare in modo inappropriato le risposte immunitarie. In linea con questo concetto, è importante valutare, da caso a caso, il ruolo dell’alimentazione e, nei casi in cui se ne prospetti la necessità, dell’integrazione mirata di componenti pro-microbiota, batteriche e non (probiotici e prebiotici). E’ stato visto altresì che una dieta troppo ricca di grassi e proteine animali e povera di fibre può alterare il microbiota intestinale e aumentare il rischio per lo sviluppo di IBD. Sebbene, anche l’eccesso di fibra e di altre sostanze come polioli, polialcol e e di oligosaccaridi può rappresentare un fattore irritante e scatenante. In ogni caso, la situazione di scompenso nota come disbiosi intestinale è attualmente considerata un possibile fattore eziologico nella patogenesi di queste malattie. I progressi tecnologici che oggi consentono una caratterizzazione più completa delle comunità microbiche intestinali, insieme a recenti studi che mostrano quanto sia importante l’impatto della dieta sulla microbiota, forniscono un forte razionale per ulteriori indagini approfondite sul legame fra cibo, microbiota e sviluppo di IBD . Pertanto, mirare a regolarizzare i pasti, moderare il consumo di alimenti di origine animale, fornire all’intestino sostanze antinfiammatorie naturali, attraverso la scelta di alimenti adeguati e/o di prodotti di integrazione (attentamente valutati da un esperto) sarebbe auspicabile in ogni caso, poiché la salute e l’equilibrio del microbiota intestinale garantiscono migliori risposte immunitarie e assorbimenti più adeguati.
alcuni fattori associati allo sviluppo di IBD possano essere rappresentati da sollecitazioni eccessive o effetti negativi sul microbiota. I fattori ambientali che possono alterarne la composizione comprendono la dieta, l’uso di antibiotici e l’area geografica. La nota “ipotesi dell’igiene” suggerisce che gli esseri umani che vivono nei paesi più industrializzati sono esposti sin dalla primissima infanzia a un minor numero di microbi che porta allo sviluppo di un sistema immunitario meno in grado di “tollerare” l’esposizione all’ambiente microbico in età avanzata. Questo può attivare in modo inappropriato le risposte immunitarie. In linea con questo concetto, è importante valutare, da caso a caso, il ruolo dell’alimentazione e, nei casi in cui se ne prospetti la necessità, dell’integrazione mirata di componenti pro-microbiota, batteriche e non (probiotici e prebiotici). E’ stato visto altresì che una dieta troppo ricca di grassi e proteine animali e povera di fibre può alterare il microbiota intestinale e aumentare il rischio per lo sviluppo di IBD. Sebbene, anche l’eccesso di fibra e di altre sostanze come polioli, polialcol e e di oligosaccaridi può rappresentare un fattore irritante e scatenante. In ogni caso, la situazione di scompenso nota come disbiosi intestinale è attualmente considerata un possibile fattore eziologico nella patogenesi di queste malattie. I progressi tecnologici che oggi consentono una caratterizzazione più completa delle comunità microbiche intestinali, insieme a recenti studi che mostrano quanto sia importante l’impatto della dieta sulla microbiota, forniscono un forte razionale per ulteriori indagini approfondite sul legame fra cibo, microbiota e sviluppo di IBD . Pertanto, mirare a regolarizzare i pasti, moderare il consumo di alimenti di origine animale, fornire all’intestino sostanze antinfiammatorie naturali, attraverso la scelta di alimenti adeguati e/o di prodotti di integrazione (attentamente valutati da un esperto) sarebbe auspicabile in ogni caso, poiché la salute e l’equilibrio del microbiota intestinale garantiscono migliori risposte immunitarie e assorbimenti più adeguati.